Vanaf 26 mei 2024 moeten alle niet-klasse I medische hulpmiddelen voldoen aan de MDR en niet meer aan de MDD. De klasse I medische hulpmiddelen moeten al sinds 26 mei 2021 conform zijn. Onder heel specifieke voorwaarden kan de transitieperiode verlengd worden waarbij de ‘Notified Body confirmation letter’ bevestigd dat de hercertificatie-proces is opgestart. In deze blog overlopen we de certificeringsprocedure voor jouw MDR-transitie. Wist je dat onze coaches je stap-voor-stap ondersteunen?
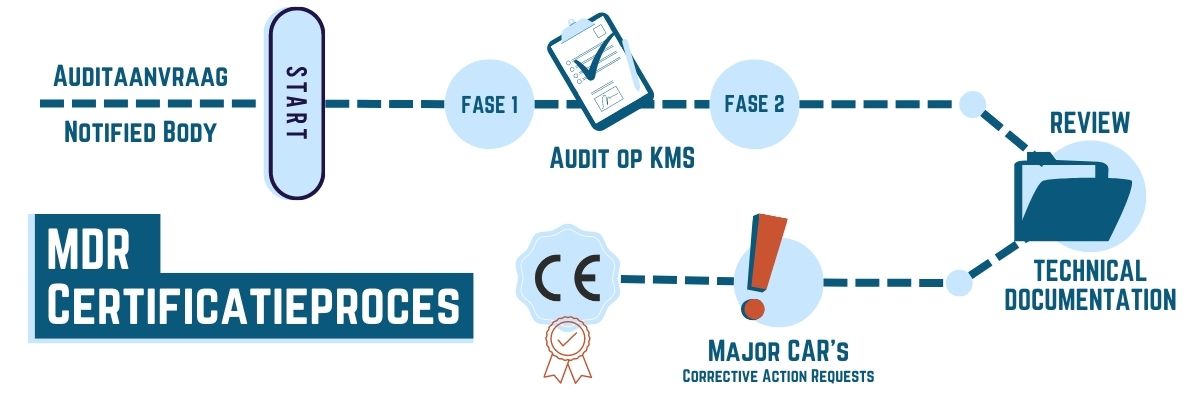
De CE-certificatie van klasse Is, Im, Ir, IIa, IIb en III hulpmiddelen starten vanaf de aanvraag van een MDR-audit bij een eigen gekozen Notified Body (NB). Klasse I medische hulpmiddelen krijgen inspecties door het Fagg en hoeven zich niet aan te melden bij een NB.
Uit ervaring weten onze coaches dat de certificeringsprocedure gemiddeld meer dan een jaar in beslag neemt. Nu beginnen aan jouw CE-certificatie is de boodschap. Heb jij jouw Notified Body al gecontacteerd? Je vindt de Notified Bodies die MDR en IVDR mogen auditeren in de NANDO dadabase. (Binnen enkele jaren wordt deze informatie uit Nando getransfereerd naar de EUDAMED database.)
Er zijn momenteel 49 NB erkend voor MDR en 12 voor IVDR, maar let vooral op de scope van hun certificaat (pagina 2 e.v.) want die is beperkt. Kijk die scope dus goed na vooraleer je een aanvraag voor CE-certificatie bij een NB indient. Klasse I medische hulpmiddelen krijgen inspecties door het Fagg en moeten geen NB contacteren.
Na akkoord door beide partijen wordt eerst een audit gepland op het kwaliteitsmanagementsysteem voor medische hulpmiddelen. Zo’n systeemaudit gebeurt doorgaans in twee fases.
De meest aangeprezen standaard om jouw KMS met de MDR te integreren is de ISO 13485:2015. Een voorbereid man, is er twee waard en onze interne auditoropleiding leert je eigenhandig de zwaktes uit jouw ISO-systeem naar bovenbrengen. Of schakel Allanta in voor een gap-analyse.
Na de systeemaudit volgt er een review van het technisch dossier. Opgelet, in april 2022 gaven 75% van Notified Bodies aan dat meer dan de helft van de ingediende documentatie onvolledig bleek (MDCG 2022-11). Het is dus bijzonder belangrijk dat je het dossier grondig voorbereidt vooraleer je een navraag indient bij een NB. In Eudamed zal later ook komen te staan wanneer een aanvraag werd geweigerd.
Bereid je de technical documentation zelf voor en zoek je een second opinion door onze MDR-kenner, wil je de nodige praktische kennis opdoen met een opleiding, of ga je voor een volledig leertraject? Allanta staat voor je klaar.
Tijdens de audits komen er ongetwijfeld minor en major non-conformiteiten naar boven die bepaalde corrigerende acties vereisen (CAR). Zodra alle major CAR’s zijn uitgevoerd ben je klaar voor de CE-certificatie. Hou er wel rekening mee dat de exacte certificatie datum onzeker is omdat de Corretive Action Request per organisatie variëren.
Met begeleiding van onze coaches maak je jouw medisch hulpmiddel stapsgewijs compliant met de MDR. En dat doen we op verschillende manieren.